Artigo traduzido e adaptado de Why is the Sea Salty and Does it Matter? de Colin A. Stedmon e André W. Visser, publicado em 11 de dezembro de 2023 pela Frontiers for Young Minds, ilustrações de Pernille W. Rasmussen. Disponível em https://kids.frontiersin.org/articles/10.3389/frym.2023.1097831. Licença de uso CC-BY-NC-4.0.
O Prof. Colin Stedmon é um oceanógrafo químico na Universidade Técnica da Dinamarca. Ele obteve seu Ph.D. pela Universidade de Copenhagen em 2004. Sua pesquisa atual se concentra na biogeoquímica marinha do Ártico. Isso envolve essencialmente estudar a composição química da água do mar e colaborar com especialistas em física e biologia marinha para entender como os oceanos funcionam e, em particular, como o Ártico está mudando. Ele gosta principalmente do trabalho de detetive. Procurando padrões nos dados, encontrando explicações para o porquê de eles estarem lá e contribuindo para uma compreensão de como os oceanos funcionam.
O Prof. André Visser é um oceanógrafo físico na Universidade Técnica da Dinamarca. Ele tem um Ph.D. em oceanografia pela Universidade Estadual de Nova York. Seus interesses de pesquisa estão onde a física e a biologia se encontram. Em particular, sua pesquisa é focada em descobrir as estratégias que o plâncton desenvolveu para prosperar no oceano, descrevendo-as com matemática para criar modelos que nos ajudem a entender o papel que elas têm em uma escala global.
Imagem de capa Pernille W. Rasmussen.
As Salinas do Rio de Janeiro
A região entre Cabo Frio, Araruama e São Pedro da Aldeia já teve cerca de 120 salinas na década de 1930 e foi, durante anos, a segunda maior produtora de sal do Brasil, perdendo apenas para o Rio Grande do Norte.
- Salina Perynas (Cabo Frio): Fundada em 1823, é considerada a primeira salina construída na região, parte da história inicial da produção de sal fluminense, atualmente um ponto de geoturismo.
- Salinas de Marrecas (Região dos Lagos): Indicada como uma das salinas selecionadas para uso geoturístico por pesquisas de 2025, ainda mantém estrutura e processos tradicionais de produção por evaporação.
- Salina Santa Mariana (Região dos Lagos): Também incluída em estudos de geoturismo como exemplo de salina ativa ou preservada, com valor histórico e paisagístico.
- Salinas da Lagoa de Araruama (conjunto histórico): A Laguna de Araruama foi descrita como o mais antigo centro salineiro do Brasil, com registros desde o século XVI.
- Salina Rio de Janeiro (empresa): Localizada no litoral fluminense e dedicada à produção sustentável de sal marinho.
Hoje, a produção fluminense é muito menor do que no passado. O Rio de Janeiro responde por cerca apenas de 2% do sal produzido no Brasil, segundo levantamento nacional.
Vamos investigar nesse artigo de onde vem o sal.
Um convite com uma pitada de sal…
Um gole de água enquanto você nada em um lago é desagradável, mas nada comparado à mesma situação durante um mergulho no oceano.
Um gole repentino de água do mar deixa você ansioso por um copo de água para lavar o gosto salgado da sua boca.
Mas você já parou para considerar por que o mar é salgado?
Neste artigo, vamos mergulhar no reino da salinidade do oceano (concentração de sal) e mostrar que há mais do que você pode ter imaginado.
De onde vem o sal do oceano?
Do que ele é feito e como a salinidade é medida?
Finalmente, por que a salinidade do oceano deveria nos interessar?
Para começar: O que é sal?
O sal é muito mais do que apenas os cristais brancos no saleiro na mesa de jantar que adicionamos à comida para torná-la mais saborosa. Vamos mergulhar um pouco mais fundo.
No oceano, quase todo o sal (97%) é composto de íons.
Um íon é um átomo ou molécula que tem uma carga elétrica porque ganhou ou perdeu elétrons.
Os íons que perderam elétrons tem carga positiva e são chamados de cátions, como o sódio (Na+1) e o magnésio (Mg 2+ ).
Os íons que ganharam elétrons tem carga negativa e são chamados de ânions, como o cloro (Cl-1) e o sulfato formado por enxofre (S) e oxigênio SO4 -2).
Os termos foram criados pelo físico-químico Michael Faraday em 1834 ao estabelecer a teoria da eletrólise. Ele usou raízes do grego antigo para nomear partículas com cargas opostas.
Cátion, vem do grego antigo káto = “para baixo”. Ânion, vem do grego antigo ánō = “para cima”.
Os íons de Sódio e Cloro formam o sal de cozinha que usamos em nossas refeições.
E todos eles são importantes e quando equilibrados e na dosagem certa, contribuem para a saúde de nosso corpo.
Mas o que temos na água do mar?
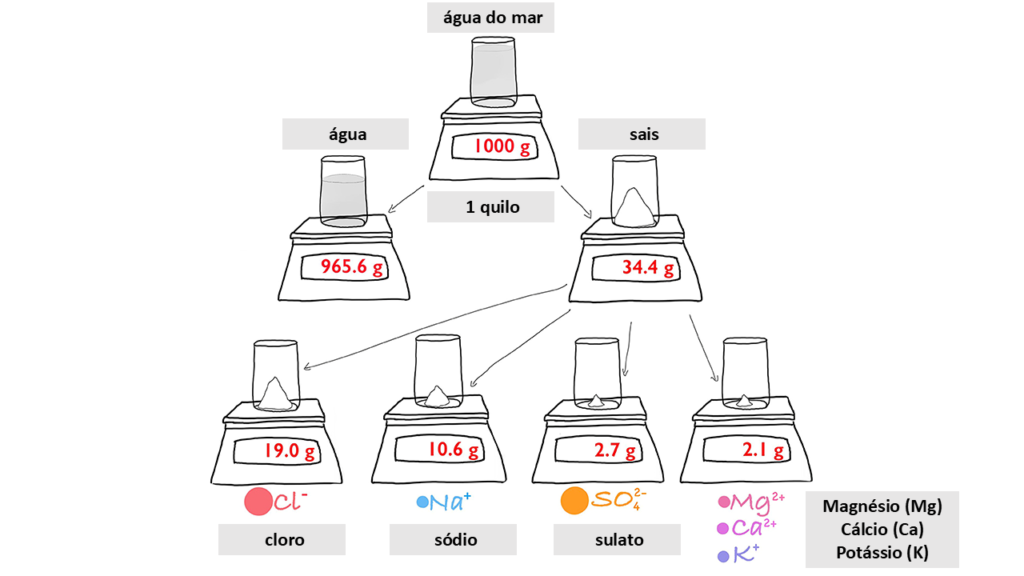
O que há em um quilo (1.000 gramas) de água do mar?
A maior parte é água, com 956,6 gramas.
O restante, um pouco mais de 34 gramas, consiste em uma coleção de sais.
Sais de Cloro (Cl – ) e de Sódio (Na + ) são os sais dominantes, representando 86% do total.
E grande parte do sal restante é o ânion sulfato (SO42-)e os cátions Magnésio (Mg 2+ ), Cálcio (Ca 2+ ) e Potássio (K +1 ) que podem se combinar para criar sais, como sulfato de magnésio e o sulfato de cálcio.
De onde vem o sal do Oceano?
O Oceano recebe a maior parte do seu sal de um processo chamado intemperismo químico das rochas ( Figura 2A ). A combinação de água da chuva, mais oxigênio (O 2 ) e dióxido de carbono (CO 2 ) do ar, atua para reagir e dissolver os minerais das rochas.
Os minerais dissolvem quando suas moléculas individuais de uma substância ficam cercadas por moléculas de um líquido, como íons de sal na água.
Você pode ver esse processo em lugares onde a água da chuva alisou superfícies de rochas, ou em estátuas ou decorações de edifícios de pedra que perderam suas formas originais.
Quando moléculas individuais de uma substância ficam cercadas por moléculas de um líquido, como íons de sal na água.
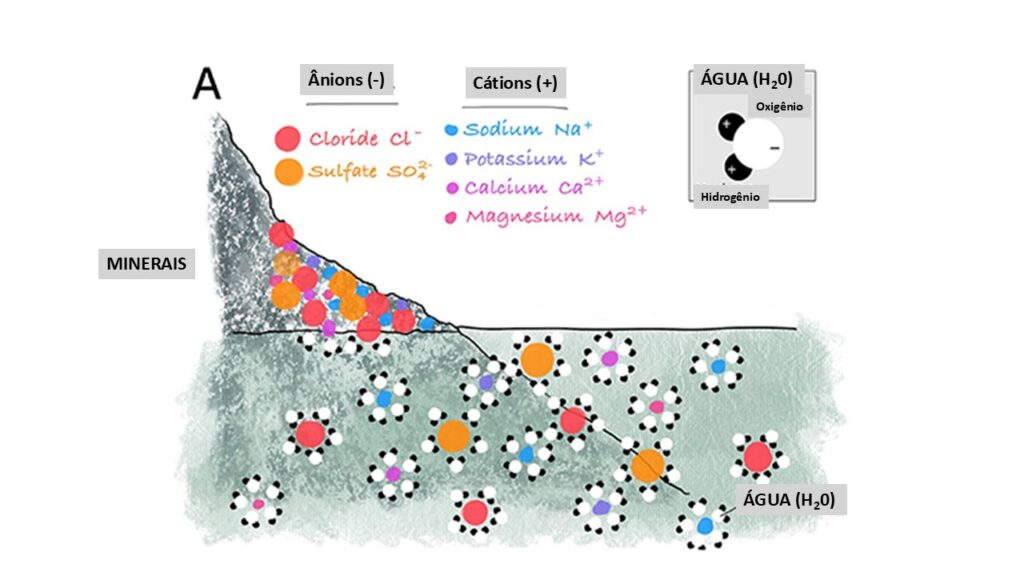
As moléculas de água têm uma carga positiva fraca em uma extremidade e uma carga negativa fraca na outra. As moléculas de água podem cercar íons de rocha, com cargas opostas atraindo e isolando os íons uns dos outros. Isso dissolve a rocha, em um processo chamado intemperismo químico da rocha.
Exemplos de intempéries são:
- A chuva ácida que dissolve calcário.
- O ferro da rocha que enferruja (oxidação).
- A água que entra na rocha e faz os minerais se decompor.
A rocha se desgasta porque seus minerais reagem quimicamente com o ambiente.
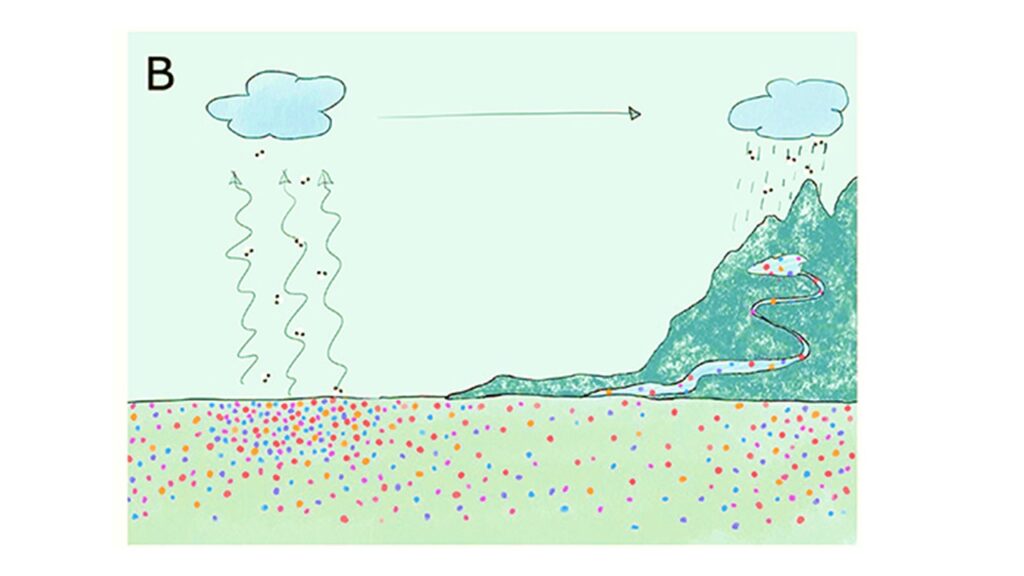
Figura 2 (B) Os sais são eventualmente levados para o oceano.
A salinidade do oceano é mais alta no oceano aberto, onde a água é perdida por evaporação e os sais dissolvidos são deixados para trás. Os rios têm baixas salinidades, e as águas costeiras geralmente ficam no meio.
A água é um excelente solvente.
As moléculas de água consistem em átomos de hidrogênio e oxigênio. A extremidade de hidrogênio da molécula de água tem uma leve carga positiva, e a extremidade de oxigênio tem uma leve carga negativa. Isso torna a água um excelente solvente – um líquido que pode dissolver um sólido ou gás.
Isso significa que ela pode dissolver íons.
Rochas e minerais contêm uma mistura de íons, que podem ser de carga negativa (ânions) e de carga positiva (cátions). Como cargas opostas se atraem, as moléculas de água cercam os íons e os isolam uns dos outros ( Figura 2A ). Então, embora a água do rio não tenha gosto salgado, ela na verdade contém sal — apenas em uma concentração muito baixa.
A concentração de sal é uma medida da quantidade de sal em um volume de líquido ou gás. Por exemplo, se tivermos 34 gramas de sal dissolvidos em 1 litro de água, dizemos que o líquido tem uma concentração de 34 gramas/litro (g/l).
Por que a água do mar é salgada?
Os rios acabam fluindo para o mar, levando consigo os sais dissolvidos da erosão das rochas ( Figura 2B ). Quando a água do oceano evapora no ar, os sais são deixados para trás. A água evaporada e cai como chuva (ou neve) sobre a terra. Esse processo se repete e fornece mais sal ao mar.
Evaporar ocorre quando as moléculas de água são aquecidas o suficiente para se afastarem umas das outras, um líquido se transforma em gás.
Mas isto deve ser apenas parte da história, caso contrário o oceano estaria aumentando cada vez mais a sua salinidade, e se tornaria tão salgados que não conseguiria dissolver mais sal.
A salinidade corresponde a concentração de sal: uma medida de quão salgada é a água do mar.
A água do mar é salgada, mas não tão salgada! Faça você mesmo!
Veja quanto sal de cozinha você consegue dissolver em 1 litro de água. Será muito mais do que as 35 gramas por litro que existem no oceano.

Numa temperatura ambiente de 25 °C, você pode dissolver cerca de 357 gramas de sal em 1 litro de água, antes que a solução fique saturada (cheia).
Isso é cerca de 10 vezes mais do que está dissolvido no oceano. Então, deve haver outros processos em jogo que removem o sal do oceano.
Os oceanógrafos chamam esses processos de “sumidouro” do sal, assim como a pia da sua cozinha remove a água que vem da torneira. O sal é lentamente removido do oceano por vários processos.
A evaporação da água em lagoas costeiras rasas pode fazer com que as concentrações de sal aumentem tanto que ele precipita e se acumula no fundo do mar. É assim que o sal marinho pode ser colhido para uso em nossa comida.
Precipitação: Quando moléculas líquidas (como água) não conseguem mais manter as moléculas de uma substância separadas umas das outras e a substância se torna sólida, como por exemplo, nos cristais de sal.
O aerossol marinho também pode mover lentamente o sal do oceano para a terra. A água no aerossol evapora e deixa o sal para trás na terra. Finalmente, a água salgada que vaza por rachaduras no fundo do oceano perto de cristas vulcânicas submarinas também remove lentamente o sal do oceano. Mas, no geral, os íons de sal permanecem no oceano milhares de vezes mais (vários milhões de anos) do que as moléculas de água (milhares de anos), tornando a água do mar mais salgada do que a água do rio.
A difícil arte de medir a Salinidade
Em todo o mundo, milhões de medições da salinidade oceânica são feitas todos os dias. Vejamos por que isso é necessário e como é feito. A salinidade e a temperatura da água do mar influenciam a densidade do oceano: a massa de um volume específico de gás, líquido ou sólido.
A densidade da água do mar é influenciada pela água, sua temperatura e a concentração de substâncias dissolvidas na água do mar. Quanto mais sal estiver dissolvido na água, mais densa ela será.
Compare:
- 1 litro de água doce a 10°C pesa 1.000 gramas,
- 1 litro de água do mar na mesma temperatura pesa 1.026 g.
As diferenças na temperatura e salinidade do oceano entre profundidades e locais influenciam as correntes oceânicas. Se quisermos entender como os oceanos afetam o clima local, o clima global e a distribuição de recursos como peixes, precisamos entender a circulação oceânica e, para isso, a salinidade desempenha um papel.
Medir a salinidade não é uma tarefa fácil, pois o sal não é uma substância, mas uma mistura.
No início das primeiras medidas oceânicas, volumes precisos de água do mar evaporavam e os sais deixados para trás eram pesados.

Na década de 1800, o geólogo dinamarquês Johan Georg Forchhammer foi mais longe e determinou as concentrações de cada sal na água, o que é um processo muito demorado, mesmo para apenas uma amostra de água.
Depois de medir cuidadosamente amostras enviadas por exploradores de todo o mundo, Forchhammer descobriu que as quantidades relativas dos vários sais na água do oceano eram quase sempre as mesmas, o que tornava as coisas muito mais simples.
Imagem: Johan Georg Forchhammer (1794-1865), Emilius Ditlev Bærentzen (cerca de 1850). Acervo Museu Copenhague. Wikipedia. Licença de Domínio Público.
Isso significava que os cientistas podiam medir apenas um sal, como o íon cloreto (Cl – ), que está presente em altas concentrações e é fácil de medir. A salinidade pode então ser calculada multiplicando-se pela constante derivada por Forchhammer: 1,812. Este número é notavelmente semelhante às estimativas modernas (1,815), o que é surpreendente, dado que ele trabalhava com equipamentos simples e nem sequer tinha iluminação elétrica!
Na década de 1960, equipamentos eletrônicos foram desenvolvidos para avaliar a salinidade medindo o quanto uma amostra de água do mar conduz eletricidade. Esta é a base dos modernos dispositivos de medição de salinidade, que podem ser montados em drones chamados Flutuadores Argo que são lançados no oceano e enviam dados de volta via satélites.
Esses drones subaquáticos têm uma coleção de sensores que podem medir pressão (para profundidade), temperatura e condutividade (para salinidade). Eles derivam com as correntes oceânicas e podem controlar o quanto eles flutuam. Quando afundam (até 2000 metros) e sobem, eles coletam medidas das propriedades da água do mar que permitem aos cientistas construir mapas da salinidade do oceano ( Figura 3 ).
Nos sites ARGO-NOOA (em https://www.aoml.noaa.gov/outreach-education/) e ARGO (em https://argo.ucsd.edu/) você pode encontrar mais informações e sugestões de atividades para sala de aula para estudar mais sobre as medidas atuais das propriedades da água do mar.

Drone submarino ARGO, usado para mergulhos de até 2000 metros e medir as propriedades do Oceano. Atualmente existem mais de 4000 drones ARGO medindo as propriedades do Oceano.
Imagem criada por IA Microsoft Copilot, 2026.

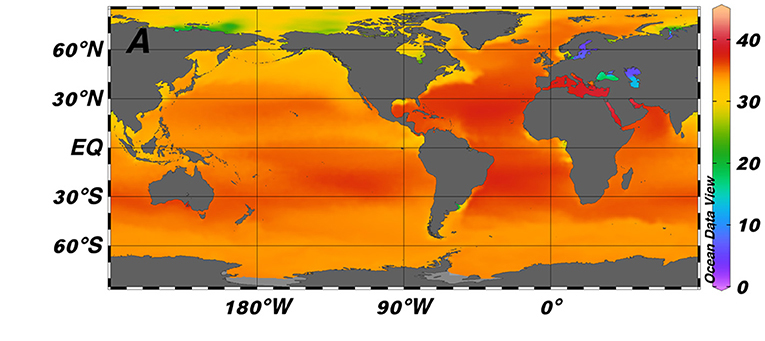
As cores vermelho-escuras mostram a maior salinidade, que geralmente ocorre nos trópicos, onde o clima quente provoca maior evaporação da água.
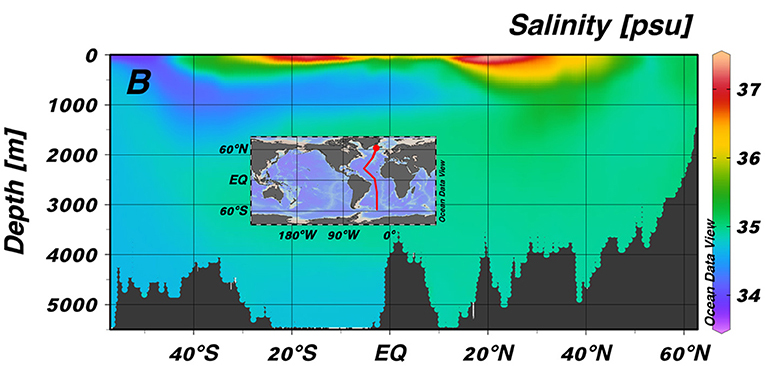
- As maiores salinidades estão nas águas superficiais dos trópicos (ambos os lados do equador).
- Em águas mais profundas, abaixo de 500 metros, a salinidade é ligeiramente menor do que na superfície (Dados do World Ocean Atlas 2018).
A história continua…
Com todo esse progresso, você pensaria que o quebra-cabeça da salinidade do oceano foi resolvido.
Mas não é o caso. Embora a ideia de Forchhammer sobre a composição constante da água do mar tenha sido enormemente útil, na verdade existem diferenças pequenas, mas mensuráveis, na composição do sal entre as regiões do oceano.
Embora essas diferenças sejam pequenas, elas são importantes se quisermos descrever com precisão as propriedades da água do mar. Então, os cientistas estão agora atualizando como calcular a salinidade do oceano, levando em consideração que os sais na água do mar não são tão constantes assim.
Depois de mais de 150 anos, a história continua a se desenrolar.
O sal é mais do que você imagina.
Lembre-se disso da próxima vez que uma onda o pegar de surpresa e você tiver um gole de água salgada!
Glossário
Íon : Um átomo ou molécula que tem uma carga elétrica porque ganhou ou perdeu elétrons. Íons carregados positivamente (Na + ) são chamados de cátions; íons carregados negativamente (Cl – ) são chamados de ânions.
Dissolver : Quando moléculas individuais de uma substância ficam cercadas por moléculas de um líquido, como íons de sal na água.
Solvente : Um líquido que pode dissolver um sólido ou gás. Água é um excelente solvente.
Concentração : A quantidade de uma substância em um volume de líquido ou gás; por exemplo, 34 g de sal em 1 L de água tem uma concentração de sal de 34 g/L.
Evaporação : Quando as moléculas de água são aquecidas o suficiente para que possam se afastar umas das outras, transformando um líquido em gás.
Salinidade : Concentração de sal; uma medida de quão salgada é a água do mar.
Precipitação : Quando moléculas líquidas (como água) não conseguem mais manter as moléculas de uma substância separadas umas das outras e a substância se torna sólida (por exemplo, cristais de sal).
Densidade : A massa de um volume específico de gás, líquido ou sólido. A densidade da água do mar é influenciada pela água, sua temperatura e a concentração de substâncias dissolvidas nela.
Conflito de interesses
Os autores declaram que a pesquisa foi conduzida na ausência de quaisquer relações comerciais ou financeiras que pudessem ser interpretadas como um potencial conflito de interesses.
Agradecimentos
Esta publicação foi apoiada por uma bolsa da Smed Foundation para AWV e Independent Research Fund Denmark Grant No. 9040-00266B para CS. As figuras foram projetadas e criadas com o apoio de Pernille W. Rasmussen.
Referências
Forchammer G. 1865. Sobre a composição da água do mar nas diferentes partes do oceano. Philos. Transact. R. Soc. Londres 155:203–62. doi: 10.1098/rstl.1865.0004
Millero FJ 2010. História da equação de estado da água do mar. Oceanografia 23:18–33.
McDougall, TJ, Jackett, DR, Millero, FJ, Pawlowicz, R., e Barker, PM 2012. Um algoritmo global para estimar a salinidade absoluta. Ocean Sci . 8:1123–34. doi: 10.5194/os-8-1123-2012.

